米托蒽醌和阿克拉霉素 髓外 aml 疗效
除了前面提到的方案外,米托蒽醌还有其他一些联合用药方案,以下是一些常用于不同疾病治疗的米托蒽醌方案: ### 急性髓系白血病(AML) - **DA - M方案** - **药物组成**:柔红霉素(DNR)、阿糖胞苷(Ara - C)和米托蒽醌(MIT)。 - **用法用量**:柔红霉素每日30 - 45mg/m²,静脉注射,第1 - 3天;阿糖胞苷每日100 - 200mg/m²,静脉滴注,第1 - 7天;米托蒽醌每日5 - 10mg/m²,静脉滴注,第1 - 3天。 - **适用情况**:对于AML患者,尤其是中高危组患者,该方案可作为诱导缓解治疗的选择之一,有助于提高缓解率。 ### 多发性骨髓瘤(MM) - **VAD - M方案** - **药物组成**:长春新碱(VCR)、阿霉素(ADM)、地塞米松(DEX)和米托蒽醌。 - **用法用量**:长春新碱每日0.4mg,持续静脉输注,第1 - 4天;阿霉素每日9mg/m²,持续静脉输注,第1 - 4天;地塞米松每日40mg,口服或静脉注射,第1 - 4天、第9 - 12天、第17 - 20天;米托蒽醌每日5mg/m²,静脉滴注,第1 - 4天。每28天为一个周期。 - **适用情况**:适用于多发性骨髓瘤的诱导治疗,特别是对于初治或复发难治性患者,可有效控制病情,提高患者的生存质量。 ### 骨肉瘤 - **MAP方案** - **药物组成**:甲氨蝶呤(MTX)、阿霉素(ADM)和米托蒽醌。 - **用法用量**:甲氨蝶呤每次8 - 12g/m²,静脉滴注,第1天,同时进行四氢叶酸钙解救;阿霉素每次30 - 40mg/m²,静脉注射,第2、3天;米托蒽醌每次10 - 15mg/m²,静脉滴注,第1天。每3 - 4周重复一次。 - **适用情况**:用于骨肉瘤的术前新辅助化疗和术后辅助化疗,可缩小肿瘤体积,提高保肢手术的成功率,降低远处转移率,改善患者的预后。 以上方案仅为常见的示例,实际临床应用中,医生会根据患者的个体差异、病情严重程度、肿瘤细胞的生物学特性等因素,对方案进行适当的调整和优化,以达到最佳的治疗效果,同时尽量减少不良反应的发生。
以下是关于HAA方案(高三尖杉酯碱+阿克拉霉素+阿糖胞苷)在急性髓系白血病(AML)中的详细解析,包括药物组成、疗效、副作用及与其他方案的对比:
HAA方案(Homoharringtonine + Aclarubicin + Cytarabine)
HAA方案是中国学者提出的AML化疗方案,尤其适用于老年患者、复发/难治性AML或存在合并症无法耐受高强度化疗者。
一、药物组成与作用机制
药物 类别 作用机制 剂量(成人标准)
高三尖杉酯碱(HHT) 植物碱类抗微管药物 抑制微管聚合,阻断有丝分裂;诱导白血病细胞凋亡,对静止期和增殖期细胞均有效。 2-3 mg/m²/d,静脉滴注(第1-7天)
阿克拉霉素(ACR) 蒽环类抗生素(第二代) 嵌入DNA双链,抑制拓扑异构酶II;心脏毒性较柔红霉素低,适合老年或心功能不全患者。 20 mg/m²/d,静脉注射(第1-7天)
阿糖胞苷(Ara-C) 抗代谢药(嘧啶类似物) 抑制DNA合成,特异性作用于S期细胞;低剂量可诱导分化,高剂量增强细胞毒性。 100-200 mg/m²/d,持续静脉滴注(第1-7天)
二、适用人群与疗效数据
适应症:
新诊断AML(尤其>60岁、体能状态较差者);
复发/难治性AML(对DA、IA方案耐药);
伴有心脏基础疾病(需避免柔红霉素/去甲氧柔红霉素的心脏毒性)。
临床疗效:
初治AML:CR率约50-65%(老年患者),中位OS 10-12个月;
复发/难治AML:ORR约30-40%,CR率20-25%;
髓外病变:对皮肤浸润、牙龈增生效果较好(CR率约35%),但对CNS浸润需联合鞘内化疗。
三、具体给药方案
疗程设计:
诱导治疗:HHT + ACR + Ara-C连用7天,间歇2-3周评估骨髓;
巩固治疗:CR后每4-6周重复1个疗程(共2-4次),剂量可调整至原剂量的80%。
剂量调整:
肝功能不全(Child-Pugh B/C):HHT减量至1.5 mg/m²/d,ACR减量至15 mg/m²/d;
肾功能不全(eGFR <30 mL/min):Ara-C减量至50 mg/m²/d。
四、副作用管理
毒性类型 常见表现 处理建议
骨髓抑制 IV级中性粒细胞减少(发生率>80%)、血小板减少 预防性使用G-CSF,必要时输注血小板。
心脏毒性 心律失常(QT间期延长)、心功能下降(发生率5-10%) 监测心电图、肌钙蛋白;避免联用其他心脏毒性药物(如氟达拉滨)。
胃肠道反应 严重恶心呕吐、黏膜炎(发生率50-70%) 使用5-HT3受体拮抗剂(如昂丹司琼),加强口腔护理。
肝损伤 转氨酶升高、胆汁淤积(发生率20-30%) 保肝治疗(谷胱甘肽、多烯磷脂酰胆碱),暂停化疗直至肝功能恢复。
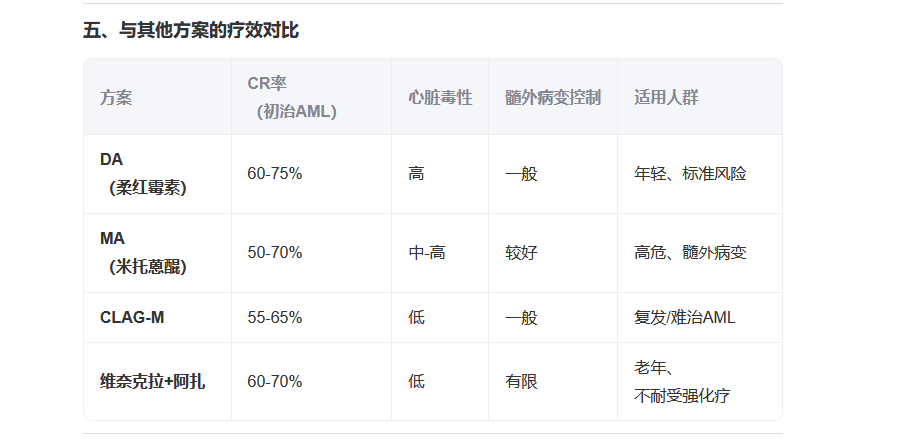
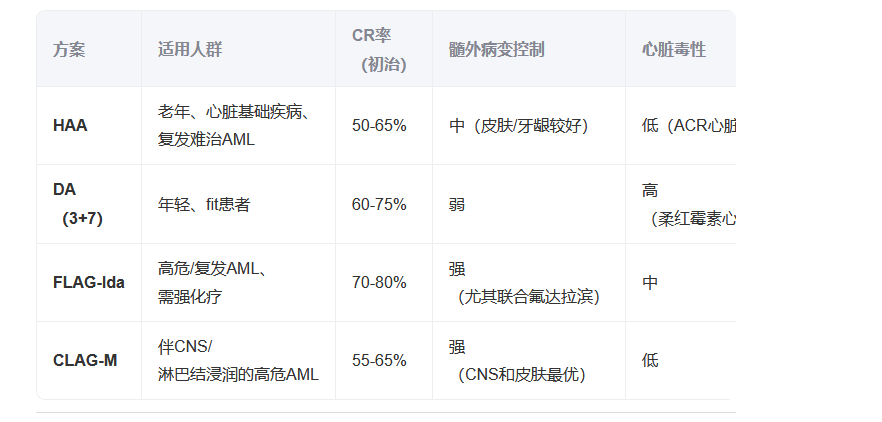
五、HAA与其他AML方案的对比
方案 适用人群 CR率(初治) 髓外病变控制 心脏毒性
HAA 老年、心脏基础疾病、复发难治AML 50-65% 中(皮肤/牙龈较好) 低(ACR心脏毒性低)
DA(3+7) 年轻、fit患者 60-75% 弱 高(柔红霉素心脏毒性高)
FLAG-Ida 高危/复发AML、需强化疗 70-80% 强(尤其联合氟达拉滨) 中
CLAG-M 伴CNS/淋巴结浸润的高危AML 55-65% 强(CNS和皮肤最优) 低
六、联合靶向治疗的优化策略
HAA + 维奈克拉(Venetoclax):
协同诱导BCL-2依赖性凋亡,适用于TP53突变或复杂核型AML;
研究数据:CR率提升至70%(复发/难治AML),需警惕骨髓抑制加重。
HAA + 去甲基化药物(地西他滨):
表观遗传学调控增强HHT的促凋亡效应;
适用老年AML:CR率60%,OS延长至14个月。
七、临床选择建议
一线选择HAA的情况:
年龄>60岁且ECOG评分≥2;
左室射血分数(LVEF)<50%或既往蒽环类药物心脏毒性史;
复发AML对FLAG/CLAG方案耐药。
慎用或禁用HAA的情况:
活动性肝炎或肝功能Child-Pugh C级;
合并严重肺部感染(HHT可能加重肺水肿);
既往对植物碱类药物过敏。
八、未来研究方向
HHT脂质体:提高药物稳定性,减少静脉炎风险(临床试验NCT04543188);
生物标志物指导:
WT1表达动态监测:预测HAA方案缓解深度;
FLT3-ITD突变:联合吉瑞替尼(Gilteritinib)提高生存率。
总结
HAA方案是中国AML治疗的重要选择,尤其适用于老年和心脏高风险患者。尽管其缓解率稍低于DA或FLAG-Ida方案,但毒性可控、性价比高。对于伴髓外病变者,可联合鞘内化疗或局部放疗;难治病例推荐联用维奈克拉或去甲基化药物。治疗中需密切监测骨髓、心脏及肝功能,及时调整支持治疗。